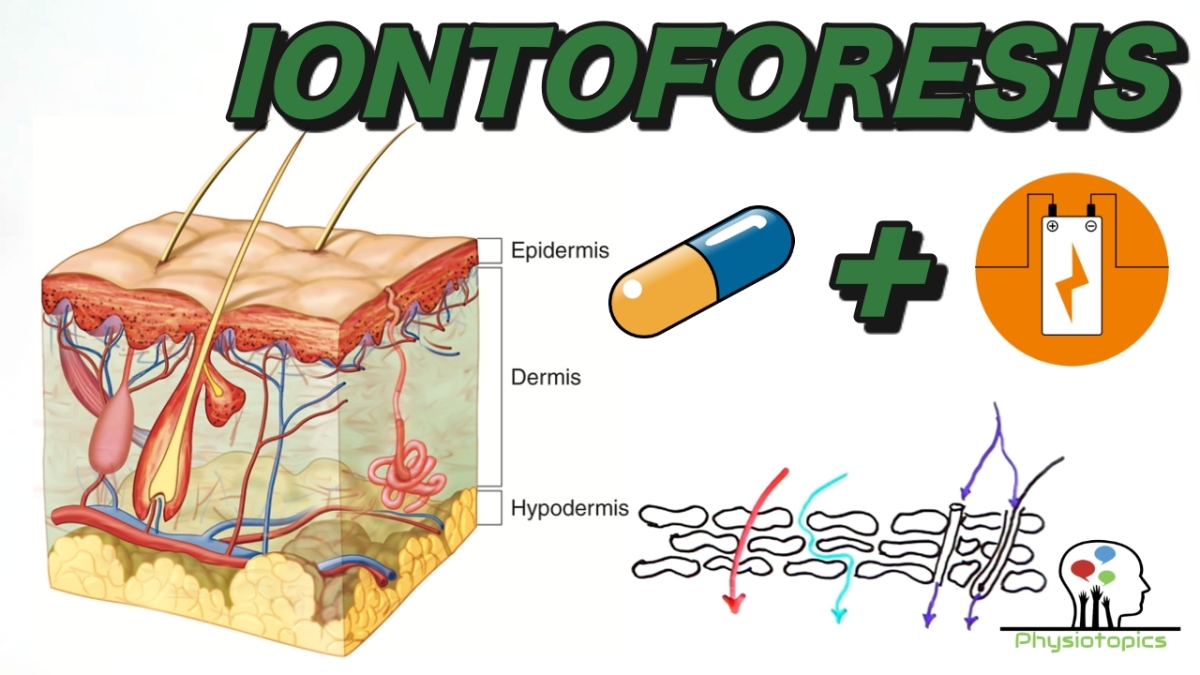
La piel es el órgano más grande del cuerpo, y junto con el cabello, las uñas, glándulas sebáceas y sudoríparas, conforma el sistema tegumentario.
Forma una barrera multicapa que rodea todo nuestro cuerpo y nos protege de factores externos como bacterias, sustancias químicas y temperatura, evitando que cualquier sustancia la atraviese y protegiendo la homeostasis del organismo (1,2).

Esta función de barrera, limita severamente la cantidad y el tipo de moléculas que pueden atravesarla tanto en un sentido como en el otro (3).
Dentro de las distintas capas que forman la piel, podemos distinguir dos principales (2):
- La dermis o capa profunda: fisiológicamente activa que forma la mayoría de lo que conocemos como piel, siendo su grosor de 1-2mm.
- La epidermis: capa superficial menos gruesa que la dermis (20–50 μm), que es fisiológicamente menos activa (4).
La capa más superficial de esta epidermis, denominada estrato córneo, está constituida por células muertas esclerosadas por su queratinización (4–6).

A pesar de su limitado grosor, este estrato forma la principal barrera para la difusión de sustancias al interior de nuestro cuerpo, debido a las diversas proteínas y lípidos que acumula en su interior y en los espacios intercelulares (5,6).
Aunque se trata de un mecanismo muy eficaz, en realidad es la piel no nos aísla completamente del medio ambiente y es parcialmente permeable.
Reflejo de esto es que el contacto físico directo de la piel con sustancias tóxicas como el dimetilmercurio puede matarnos.
Existen 2 formas principales de absorción a través de la piel (6,7):
- Transepidérmica: dentro de la cual podemos distinguir la vía
- Transcelular: la sustancia atraviesa los corneocitos
- Intercelular: la sustancia se difunde a través de los espacios intercelulares
- Transapendicular: a pesar de ser una vía más rápida, (mayor diámetro=menor resistencia), ofrecen una superficie muy limitada (1%)
- Transfolicular: cuando la sustancia penetra a través de los folículos pilosos
- Transudorípara: a través de los poros y conductos que conectan las glándulas sudoríparas a la superficie

Debido a esta baja permeabilidad de la piel, siempre se han buscado maneras facilitar la penetración de sustancias a través de la misma, con especial interés en casos como la administración de fármacos.
La idea de introducir substancias con carga eléctrica en la piel a través del uso de la electricidad se le atribuye a Veratti en 1747. Años después (1898) Morton realizó un experimento en el que introdujo grafito en polvo en su brazo a través de este método, apareciendo pequeños puntos negros que se mantuvieron durante semanas (8).

A pesar de estos antecedentes, se considera que los primeros experimentos bien documentados se realizaron a principios del siglo XX, por LeDuc (1908) (8).
En su clásico experimento, utilizó dos conejos conectados en serie a una corriente directa. Puso estricnina entre el electrodo positivo y la piel en uno de ellos y cianuro entre el electrodo negativo y la piel del otro conejo.
Observó qué iones se habían introducido a través de la piel observando los signos en cada uno de ellos. Los resultados fueron bastante dramáticos observándose convulsiones tetánicas en el conejo de la estricnina y muerte con síntomas de envenenamiento por cianuro en el otro (8).

Después cogió otros dos conejos y repitió el experimento cambiando la polaridad de la corriente. En esta ocasión, ninguno de los conejos murió, concluyendo que la estricnina fue atraída y no repelida del electrodo negativo, y el cianuro atraído y no repelido hacia el electrodo positivo (9).

Hoy hablaremos sobre la iontoforesis, que consiste en la utilización de una corriente eléctrica de baja amplitud para facilitar la administración transdérmica (a través de la piel) de los fármacos de forma no invasiva (2,10,11).
Para entender la iontoforesis, debemos saber primero que los compuestos inorgánicos, en soluciones acuosas, se disocian en cationes con carga positiva y aniones con carga negativa.
Cuando se les aplica una corriente directa, los iones con carga positiva por ejemplo, son repelidos del polo positivo y son atraídos hacia el polo negativo. En el caso de los iones con carga negativa ocurre justo lo contrario (12,13).

Esta regla en la que las cargas opuestas se atraen y las cargas similares se repelen es la base de la iontoforesis (2).
En la iontoforesis ocurren tres mecanismos físicos principales (14):
- Electro-repulsión: las sustancias con carga similar son repelidas de los electrodos como consecuencia del campo eléctrico
- Permselectividad: el flujo de la corriente aumenta la permeabilidad de la piel
- Electroosmosis: la diferencia de potencial entre los electrodos provoca un flujo electroosmótico
ELECTRO-REPULSIÓN
Si alguna vez has jugado con imanes, comprobarías que es prácticamente imposible unir dos por el extremo del mismo nombre. Es decir, juntar dos positivos o dos negativos debido a que la fuerza que se genera entre ambos es repulsiva y no de atracción.
Con las cargas eléctricas ocurre algo similar. Podríamos decir que al colocar un fármaco con iones de carga negativa entre la piel y el electrodo negativo, esté fármaco es repelido, e intentará alejarse del electrodo, siendo su única opción penetrar en la piel.
PERMSELECTIVIDAD
Para entender el segundo mecanismo, es interesante saber que la piel sería isoeléctrica, es decir sin carga, a un pH entre 3 y 4. Pero a un pH fisiológico, la piel suele tener carga negativa, que favorece la penetración de los iones positivos. Siendo ésta, la principal razón por la que es más fácil introducir en la piel sustancias con carga positiva (12).
Sin embargo, se ha visto que el paso de corriente a través de la piel puede modificar su pH y por tanto su permselectividad, facilitando el transporte de distintas sustancias (14).
ELECTRO-ÓSMOSIS
Si estos fueran los únicos mecanismos por los que una sustancia atraviesa la piel, sólo podrían atravesarla sustancias ionizadas con carga, ya sea positiva o negativa, mientras que la mayoría de las sustancias orgánicas se quedarían fuera. El proceso físico a través del cuál las sustancias sin carga pueden llegar a atravesar la piel se denomina electroósmosis, o iontohidrocinesia. A pesar de que la corriente eléctrica actúa sobre las sustancias con carga, este flujo de iones “empuja” al resto de las sustancias del solvente al chocar con estas moléculas en su camino hacia el electrodo con carga opuesta, favoreciendo que éstas también sean absorbidas (12,14).
A pesar de la ayuda de estos mecanismos, la piel sigue siendo una excelente barrera por lo que no podemos hacer pasar cualquier tipo de fármaco a través de ella. La sustancia que queramos introducir debe cumplir ciertos requisitos como que pueda ser ionizada y estable en una solución, que no sea alterada por el paso de la corriente eléctrica o que sus iones sean de un tamaño pequeño o moderado (10).

Ahora que entendemos cómo se transportan los fármacos a través de la piel con ayuda de la corriente eléctrica, puede que nos preguntemos, cómo se hace de forma práctica y qué parámetros debemos decidir para su correcta utilización (10):
TAMAÑO Y COLOCACIÓN DEL ELECTRODO
Se suelen utilizar electrodos de silicona cubiertos con una esponja o gamuza humedecida, para favorecer el paso de la corriente eléctrica.
Distintos fármacos suelen venir ya disueltos en concentraciones óptimas para su aplicación, y se deben colocar entre el electrodo y la piel.
El tamaño del electrodo vendrá determinado, entre otros, por el área que queramos tratar en función de la estructura lesionada. Es importante tener en cuenta este tamaño ya que será lo que determine cuánto podemos subir la intensidad después, disminuyendo el riesgo de provocar quemaduras (10).
POLARIDAD
Para saber debajo de qué electrodo debemos colocar el fármaco, debemos conocer primero su carga. Si vamos a aplicar diclofenaco sódico por ejemplo, sabiendo que su carga es negativa, deberemos colocarlo entre el electrodo negativo y la piel, para que el paso de la corriente lo aleje del electrodo y lo empuje hacia la piel.
INTENSIDAD
A pesar de haber unos límites por seguridad en cuanto a intensidad en mA por cm2 del electrodo que hayamos utilizado, lo que realmente manda es la sensación del paciente.
No debería notar picor ni quemazón con la aplicación de la corriente, ya que sería un signo previo de que se está produciendo una quemadura en la piel.
Nos gustaría trasladar una reflexión interesante en la que estos límites de intensidad que habitualmente se definen en 0,1-0,2 mA/cm2de electrodo, suelen estar sacadas de la aplicación de la corriente continua para obtener efectos galvánicos, pero en la iontoforesis convendría quedarse por debajo ya que se trata de introducir un fármaco, y no de provocar efectos galvánicos (9).

TIPO DE CORRIENTE
Si bien se pueden utilizar distintas corrientes, la más utilizada es la corriente continua o directa, debido al flujo constante de empuje que provoca sobre el fármaco, teniendo siempre precaución para no provocar quemaduras.
TIEMPO DE TRATAMIENTO
El tiempo durante el que vayamos a aplicar la corriente depende de forma directa de la intensidad que hayamos aplicado.
Una de las principales desventajas de la iontoforesis en comparación a otras técnicas es que resulta difícil medir la dosis que ha penetrado en la piel.
Lo que sí que podemos medir con exactitud es la cantidad de electricidad utilizada para para la iontoforesis en mA-min. Es decir, multiplicando la intensidad utilizada por el número de minutos durante el cuál se ha aplicado.
Algunos autores han demostrado una transmisión efectiva de fármacos con aplicaciones de 40-80 mA-min para cada aplicación de iontoforesis (10).
Por tanto, si hemos subido la intensidad a 2mA por ejemplo, y queremos aplicar un tratamiento de 40mA-min, deberíamos aplicarla durante 20 minutos.
Los aparatos más avanzados, realizan el cálculo de forma automática. A medida que aumentamos la intensidad, reducen el tiempo de aplicación.

CONTRAINDICACIONES
La iontoforesis no debería ser aplicada por prudencia en los siguientes casos (15):
- En personas con trastornos sensoriales superficiales y profundos, ya que correríamos el riesgo de provocar una quemadura
- En caso de hipersensibilidad al fármaco utilizado
- Y tampoco se recomienda su utilización durante el embarazo y la lactancia
DESVENTAJAS
Las principales desventajas de la iontoforesis podrían resumirse en:
- La dificultad de estabilizar el agente terapéutico en el vehículo de aplicación
- Complejidad del sistema de liberación del fármaco
- Exposición prolongada de la piel a la corriente eléctrica
VENTAJAS
Sin embargo, las ventajas superan con creces a las desventajas (12,16):
- Evitando los riesgos e inconvenientes de la aplicación parenteral
- Previniendo la variación el absorción y metabolizado observado en la aplicación oral
- Aumenta la eficacia terapéutica al evitar que el fármaco pase por el hígado y sea eliminado en parte, antes de llegar al tejido diana, como ocurre cuando ingerimos
- Disminuye las opciones de pasarnos con la dosis o de quedarnos cortos a través de una administración continua del fármaco
- Permite el uso de fármacos con una vida media biológica corta al pasar directamente a la sangre sin pasar por el intestino ni hígado
- Su aplicación es sencilla e indolora lo que aumenta la adhesión o conformidad del paciente con el tratamiento

Resumiendo, podríamos decir que la iontoforesis es una buena alternativa para la administración de fármacos a través de la piel.
Se trata de una tecnología que se sigue desarrollando hoy en día, en combinación a otros métodos físicos y químicos, para aumentar el número y variedad de sustancias que podemos introducir de forma efectiva (6,10).
Entre sus futuros retos podríamos nombrar, el poder controlar de forma más precisa la dosis aplicada, y su posible utilización de forma inversa para obtener los valores sanguíneos de ciertas substancias sin necesidad de atravesar la piel del forma agresiva (10).
Como siempre os dejamos la versión en video por aquí:
Hasta pronto 😉
BIBLIOGRAFÍA:
1. Capas de la piel: MedlinePlus enciclopedia médica illustración [Internet]. Disponible en: https://medlineplus.gov/spanish/ency/esp_imagepages/8912.htm
2. Filipovic N, Zivanovic M, Savic A, Bijelic G. Numerical simulation of iontophoresis in the drug delivery system. Comput Methods Biomech Biomed Engin. 2016;19(11):1154-9.
3. Guy RH. Iontophoresis–recent developments. J Pharm Pharmacol. abril de 1998;50(4):371-4.
4. Giri TK, Chakrabarty S, Ghosh B. Transdermal reverse iontophoresis: A novel technique for therapeutic drug monitoring. J Control Release Off J Control Release Soc. 28 de 2017;246:30-8.
5. Pons L. Estrato córneo. Offarm. 1 de febrero de 2004;23(2):166-8.
6. Chaulagain B, Jain A, Tiwari A, Verma A, Jain SK. Passive delivery of protein drugs through transdermal route. Artif Cells Nanomedicine Biotechnol. 2018;46(sup1):472-87.
7. Sánchez-Saldaña LA. Absorción percutánea. Artículo de revisión. Percutaneous absorption. Soc Peru De [Internet]. Disponible en: https://www.dermatologiaperuana.pe/assets/uploads/revista_h45A_03_Articulo_revision_28-2.pdf
8. Chien YW, Banga AK. Iontophoretic (transdermal) delivery of drugs: overview of historical development. J Pharm Sci. mayo de 1989;78(5):353-4.
9. Martín JMR. Electroterapia En Fisioterapia. Ed. Médica Panamericana; 2004. 668 p.
10. Cameron Michelle. Physical Agents in Rehabilitation – 5th Edition [Internet]. Saunders; 2017. 464 p. Disponible en: https://www.elsevier.com/books/physical-agents-in-rehabilitation/cameron/978-0-323-44567-2
11. Krueger E, Junior C, Luiz J, Scheeren EM, Neves EB, Mulinari E, et al. Iontophoresis: principles and applications. Fisioter Em Mov. septiembre de 2014;27(3):469-81.
12. Costello CT, Jeske AH. Iontophoresis: applications in transdermal medication delivery. Phys Ther. junio de 1995;75(6):554-63.
13. Cosmetics and Skin: Iontophoresis [Internet]. . Disponible en: https://www.cosmeticsandskin.com/cdc/iontophoresis.php
14. Naik null, Kalia null, Guy null. Transdermal drug delivery: overcoming the skin’s barrier function. Pharm Sci Technol Today. 1 de septiembre de 2000;3(9):318-26.
15. Karpiński TM. Selected Medicines Used in Iontophoresis. Pharmaceutics. 25 de octubre de 2018;10(4).
16. Dixit N, Bali V, Baboota S, Ahuja A, Ali J. Iontophoresis – an approach for controlled drug delivery: a review. Curr Drug Deliv. enero de 2007;4(1):1-10.